科学家揭示了两种加剧帕金森病进展的蛋白质
两种蛋白质可能与帕金森病的进展密切相关,帕金森病是一种无情且致残的神经退行性疾病,影响着全世界数百万人。
科学家们正在竞相寻找有关这种疾病的新线索,随着全球人口不可阻挡的老龄化,患病率正在增加。大多数病例发生在 60 岁以后,但估计 5%-10% 是 50 岁之前发生的早发型疾病。这些病例通常(但不完全)与从一代传给下一代的基因突变有关。
帕金森氏症的特点是大脑基底神经节退化和重要神经递质多巴胺缺乏。震颤是该疾病的特征性症状,肌肉强直和步态缓慢、不精确也是该病的特征性症状。尽管这些症状很严重,但患者会进一步受到一系列复杂而不同的非运动症状的影响,这些症状会极大地影响他们的生活质量。
根据美国非营利组织帕金森基金会的说法,抑郁、焦虑、冷漠、幻觉、便秘、睡眠障碍、嗅觉丧失和各种认知障碍会使患者应对病情的能力复杂化,帕金森基金会是一家美国非营利组织,为患者及其家人提供信息资源。
一项新的研究将注意力集中在该疾病背后的关键分子机制上,阐明了一对加剧疾病进展的蛋白质之间的联系。
波士顿布莱根妇女医院Ann Romney神经疾病中心的Gary P.H. Ho博士及其同事将这些蛋白质确定为突触受体-11-Syt11-和α-突触核蛋白,通常写为α-突触核蛋白。这种叛逆的配对可能有助于该疾病的标志性细胞病理学,Ho及其同事发现。
这项新研究揭开了α-突触核蛋白(大脑中帕金森病的核心驱动因素)与Syt11之间的生化联系,并可能解释为什么Syt11以前与该病有关,但其作用直到现在仍未确定。对Syt11活性的新深入研究与α-突触核蛋白一起微调了对Syt11的科学理解。
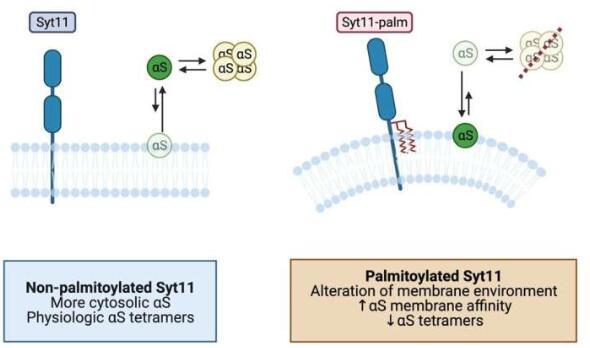
“我们调查了这两种蛋白质是否有联系,”该研究的第一作者Ho写道,该研究发表在《科学信号》杂志上。“我们发现Syt11在小鼠和人类脑组织以及培养的皮质神经元中被棕榈酰化,并且对Syt11的这种修饰破坏了神经元中的α-突触核蛋白稳态。
棕榈酰化是脂肪酸(如棕榈酸)与半胱氨酸(较少见于丝氨酸和苏氨酸)的共价附着。在这项研究中,Ho及其同事发现棕榈酰化影响了Syt11上的两个半胱氨酸残基,这导致蛋白质移动到神经元中细胞内膜的区域,在那里它不能被降解。其他实验表明,Syt11的棕榈酰化破坏了神经元中α-突触核蛋白的调节,并提高了容易聚集,疾病相关的α-突触核蛋白形式的丰度。
“在神经元中,Syt11的棕榈酰化增加了其丰度并增强了α-突触核蛋白与细胞内膜的结合,”Ho补充道。“结果,α-突触核蛋白的生理四聚体形式的丰度降低,其聚集倾向的单体形式的丰度增加。
在这项研究中,Ho和他的合作者研究了帕金森氏症动物模型以及人类捐赠者的脑组织。根据《科学信号》的数据,这两种有害蛋白质的影响“在小鼠的原代神经元以及来自健康供体和家族性帕金森病患者的细胞的神经元中”可见。
虽然这项研究为理解帕金森病背后的分子机制打开了一扇新的窗口,但这种毁灭性疾病的原因仍然难以捉摸,并且无法治愈。神经退行性疾病可能具有少数人的家族根源,其诊断由基因突变解释。对于大多数人来说,这种疾病的表现没有明显的原因,尽管科学家认为接触杀虫剂或除草剂可能起作用。
近年来的一系列研究在了解该疾病的核心机制和遗传风险因素方面取得了长足的进步。例如,全基因组关联研究已将编码Syt11的基因与帕金森病的高风险联系起来。
现在,波士顿团队,Dennis Selkoe博士实验室的所有同事,通过展示两种蛋白质如何相互联系,将Syt11和α-突触核蛋白之间的联系进一步迈出了诱人的一步。
根据总部位于迈阿密和纽约市的帕金森基金会的数据,全球有超过10万人患有帕金森病。该疾病的主要药物是左旋多巴,它治疗疾病的运动症状。神经元处理药物以补充缺失的多巴胺。其他药物,如卡比多巴,有助于在无情的疾病进展中支持大脑。
与此同时,Ho及其同事认为,他们的研究正在为帕金森病的整体理解增加一个新的维度。“这项工作开始为Syt11在疾病中的作用带来机制清晰度,并提供进一步的证据,证明棕榈酰化影响[α-突触核蛋白]生物学中的多种途径,”Ho总结道。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【禁不住念什么】在日常生活中,我们常常会遇到一些词语让人“禁不住”去读、去想,甚至去写。其中,“禁不住...浏览全文>>
-
【禁闭岛结局】《禁闭岛》(英文名:Shutter Island)是一部由马丁·斯科塞斯执导,莱昂纳多·迪卡普里奥主演...浏览全文>>
-
【禁闭岛的结局真相】《禁闭岛》(英文名:Shutter Island)是一部由马丁·斯科塞斯执导,莱昂纳多·迪卡普里...浏览全文>>
-
【靳字怎么读】在日常生活中,我们经常会遇到一些不常见的汉字,这些字不仅发音复杂,含义也常常让人感到困惑...浏览全文>>
-
【靳这个字怎么念】“靳”是一个较为少见的汉字,常用于人名或姓氏中。对于不熟悉该字的人来说,可能会不知道...浏览全文>>
-
【靳怎么读音】“靳”是一个较为少见的汉字,常出现在人名或地名中。对于不熟悉这个字的人来说,可能会对其读...浏览全文>>
-
【靳东个人资料】靳东是中国内地著名的男演员,因在多部影视作品中表现出色而广受观众喜爱。他以沉稳的气质、...浏览全文>>
-
【靳东的妹妹为什么叫高露】很多人对“靳东的妹妹为什么叫高露”这一问题感到疑惑,因为从名字上看,似乎“高...浏览全文>>
-
【金枝玉叶剧情简介】《金枝玉叶》是一部以民国时期为背景的都市情感剧,讲述了出身名门的女主角在家族、爱情...浏览全文>>
-
【金枝玉叶花语是什么】“金枝玉叶”是一种常见的观赏植物,因其叶片厚实、色泽翠绿、形态美观而广受喜爱。在...浏览全文>>
