极其罕见的基因变异指出了年龄相关性黄斑变性的潜在原因
美国国家眼科研究所(NEI)的一项研究确定了罕见的遗传变异,这些变异可能指向驱动年龄相关性黄斑变性(AMD)的一般机制之一,AMD是老年人视力丧失的常见原因。
这些变体产生畸形的蛋白质,改变膜攻击复合体(MAC)的稳定性,这可能会驱动视网膜的慢性炎症反应。发表在《iScience》杂志上的研究结果指出,MAC是减缓或预防AMD发展的潜在治疗靶点。NEI是美国国立卫生研究院的一部分。
有许多已知的遗传变异可以提高或降低个体患AMD的风险;然而,这些遗传变化中的每一个对AMD的贡献都很小。
为了发现与疾病直接相关的遗传变异和蛋白质,NEI神经生物学,神经变性和修复实验室主任,该研究的主要作者Anand Swaroop博士与俄勒冈健康科学大学(OHSU)的AMD临床医生Michael Klein博士合作。Klein收集了数百名患者的临床信息,以及AMD患者人数众多的家庭。
Swaroop,Klein及其同事寻找携带非常罕见的AMD致病变异的家族,其中基因变异的影响非常强,并且变异直接影响蛋白质结构和功能。这种类型的罕见变异可以揭示疾病的根本原因。
“虽然我们已经知道许多影响AMD风险的遗传变异,但只有少数直接指出可能导致AMD的蛋白质改变,”Swaroop说。
“通过观察具有超罕见变异的大家庭,这些变异与几代人的疾病密切相关,我们发现两种蛋白质可能直接是受影响患者AMD病理学背后的驱动力。这些蛋白质可能是未来药物的靶标。虽然目前有一些治疗方法可以减缓湿性AMD患者的视力丧失,但大多数患者没有治疗方法,也没有治愈这种疾病的方法。
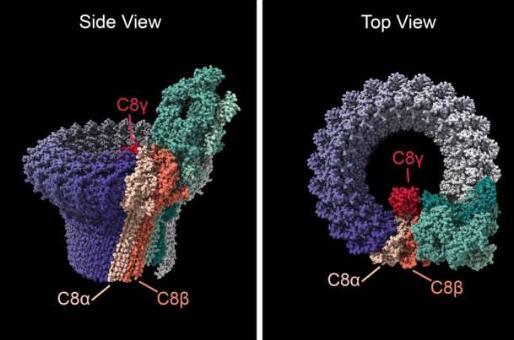
Swaroop,Klein及其同事发现,在四个家庭中,患有AMD的个体在形成MAC一端的两种蛋白质之一中发生突变:C8-α和C8-β。研究小组发现,来自四个AMD家族的变异都影响了C8蛋白相互粘附的能力,这可能会改变MAC在眼睛视网膜中的行为方式。
MAC形成一个圆形孔,一端被C8蛋白封闭;MAC孔允许离子流过细胞的外膜。这个毛孔是“补体级联”的最后一步,补体级联是免疫系统的一部分,帮助身体抵御病原体。尽管科学家最初认为MAC的唯一功能是插入细菌细胞膜并杀死病原体,但最近的证据表明MAC在调节视网膜等组织的炎症过程中起着复杂的作用。
来自NEI年龄相关眼病研究的遗传数据表明,C8蛋白以及补体级联中较高位置的其他蛋白质在AMD中的作用。由于MAC是补体级联的最后一步,因此影响任何补体蛋白的变异可能会向下漏斗以改变MAC功能。研究人员认为,视网膜中稳定MAC过多或过少都可能导致破坏性炎症,进而推动AMD进展。
“鉴于MAC是免疫系统补体途径的终点,并且因为这些罕见的变异与疾病之间存在如此密切的联系,我们认为靶向它可能是控制AMD的更有效策略,”Swaroop说。“使用小分子药物,我们可能能够控制MAC驱动炎症的强度,并从那里减缓AMD的进展。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【禁不住念什么】在日常生活中,我们常常会遇到一些词语让人“禁不住”去读、去想,甚至去写。其中,“禁不住...浏览全文>>
-
【禁闭岛结局】《禁闭岛》(英文名:Shutter Island)是一部由马丁·斯科塞斯执导,莱昂纳多·迪卡普里奥主演...浏览全文>>
-
【禁闭岛的结局真相】《禁闭岛》(英文名:Shutter Island)是一部由马丁·斯科塞斯执导,莱昂纳多·迪卡普里...浏览全文>>
-
【靳字怎么读】在日常生活中,我们经常会遇到一些不常见的汉字,这些字不仅发音复杂,含义也常常让人感到困惑...浏览全文>>
-
【靳这个字怎么念】“靳”是一个较为少见的汉字,常用于人名或姓氏中。对于不熟悉该字的人来说,可能会不知道...浏览全文>>
-
【靳怎么读音】“靳”是一个较为少见的汉字,常出现在人名或地名中。对于不熟悉这个字的人来说,可能会对其读...浏览全文>>
-
【靳东个人资料】靳东是中国内地著名的男演员,因在多部影视作品中表现出色而广受观众喜爱。他以沉稳的气质、...浏览全文>>
-
【靳东的妹妹为什么叫高露】很多人对“靳东的妹妹为什么叫高露”这一问题感到疑惑,因为从名字上看,似乎“高...浏览全文>>
-
【金枝玉叶剧情简介】《金枝玉叶》是一部以民国时期为背景的都市情感剧,讲述了出身名门的女主角在家族、爱情...浏览全文>>
-
【金枝玉叶花语是什么】“金枝玉叶”是一种常见的观赏植物,因其叶片厚实、色泽翠绿、形态美观而广受喜爱。在...浏览全文>>
