研究发现清除错误折叠蛋白质的新途径
为了找到新的途径,人文与科学学院唐纳德·肯尼迪朱迪思·弗里德曼(Judith Frydman)实验室的研究人员整合了几种遗传,成像和生化方法,以了解酵母细胞如何处理错误折叠的蛋白质。在实验中,研究小组将错误折叠的蛋白质限制在细胞核或细胞质 - 细胞内但细胞核外的区域。该团队通过活细胞成像和超分辨率显微镜直观地跟踪错误折叠蛋白质的命运。
“第一件事令人兴奋的是,我们实际上发现细胞核和细胞质之间存在通信,”该论文的共同主要作者,弗莱德曼实验室的前博士后学生Emily Sontag说。 “所以他们互相告诉对方,'我们都有很多错误折叠的蛋白质;让我们协调将它们送到这个垃圾场,以便可以将它们移除。
研究小组将“垃圾场”位点确定为细胞核和液泡的交集 - 一个充满降解蛋白质的酶的细胞器 - 并表明在这个“垃圾场”地点的错误折叠蛋白质被移动到液泡内部进行降解。他们还表明,该途径取决于一类用于产生小囊泡以在细胞周围运输分子的蛋白质。
“将这个特定的蛋白质家族和囊泡交通生物学的这一方面与蛋白质清除联系起来,为我们提供了一种看待阿尔茨海默氏症,帕金森氏症,亨廷顿氏症 - 所有这些神经退行性疾病的新方法,”桑塔格说。
细胞核和细胞质的共享“垃圾场”站点
细胞可以通过两种方式处理错误折叠的蛋白质:通过重新折叠它们或消除它们。第三种选择是将它们存储在特定的蜂窝位置。
“当细胞决定是否重新或降解蛋白质时,它会将它们隔离到这些无膜内含物中,”该论文的资深作者Frydman说。内含物是出现在细胞质和细胞核中的错误折叠蛋白质簇。
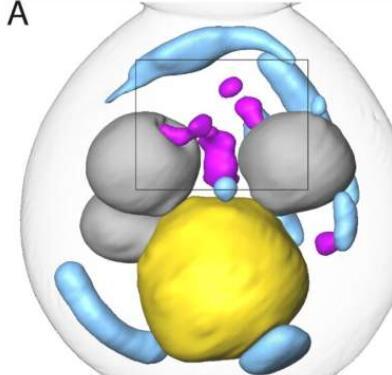
研究小组发现,细胞机器在细胞核和细胞质内的不同位置形成小的错误折叠蛋白质内含物,就像微小的垃圾场一样,然后向细胞核和液泡之间的边界迁移,这是一个更大的垃圾场。最终,核和细胞质错误折叠的蛋白质包涵体排列成彼此面对,核包膜将它们分开。
“细胞核和细胞质之间的来回通信根本不是我们预期的,”桑塔格说。“知道这两个隔间可以协同工作,从任何地方清除垃圾,真的很棒。
“这表明细胞核中错误折叠蛋白质的管理和细胞质中错误折叠蛋白质的管理是不同的,但是协调的,”Frydman说。“真正酷的是,每个隔室都将错误折叠的蛋白质移动到核包膜与液泡膜相遇的部位。
从垃圾场到退化:新的途径
酵母中的液泡相当于哺乳动物细胞中的溶酶体。它是一种膜结合的细胞器,充满了分解蛋白质的酶 - 细胞的回收中心。
“这不是随机的,”该论文的共同主要作者,Frydman实验室的博士后学者Fabián Morales-Polanco说。“细胞将内含物带到同一个地方是有原因的。
研究小组怀疑原因是将内含物送到液泡中进行降解,但这引发了进一步的问题。细胞质包涵体很容易通过自噬进入液泡,自噬是细胞用来将物质从细胞质中拉入液泡或溶酶体的过程。但在原子核中,内含物通过核包层与液泡分离。
“即使他们来到同一个地方,他们也不会通过同一扇门进入液泡,”莫拉莱斯 - 波兰科说。
为了研究受损蛋白质进入液泡的途径,研究小组阻断了蛋白酶体 - 另一种主要的蛋白质清除机制 - 并监测剩余的蛋白质清除活性。他们还使用低温软X射线断层扫描和荧光显微镜数据创建了含有这些错误折叠蛋白质内含物的细胞的3D图像。
他们发现,正如预期的那样,细胞质内含物确实推入了液泡。但核内含物的路线令人惊讶。核内含物直接从细胞核萌芽到两个膜连接处的液泡中。通过一系列遗传实验,研究小组表明,ESCRT II / III和Vps4蛋白促进了出芽进入液泡的作用。已知这些蛋白质会导致膜弯曲和“发芽”,或在其他过程中形成新的囊泡,但尚未被研究为有助于清除受损蛋白质的细胞核。它们可能是错误折叠蛋白质疾病的有吸引力的治疗靶点。
最后,使用pH敏感标签,该团队实际上将内含物跟踪到液泡中。
“我们能够看到这些错误折叠的蛋白质进入液泡,并表明这确实是一条新的途径,”Morales-Polanco说。
关注衰老
该团队在酵母细胞中进行这些实验,酵母细胞易于生长且繁殖迅速。下一步是研究哺乳动物细胞中是否使用相同的途径来清除人类疾病相关蛋白质。
下一步是定义细胞核和细胞质之间的通信如何沿着途径发生,另一个步骤是观察该途径如何受到衰老的影响。
“有很多证据表明,这种处理错误折叠蛋白质的过程会随着年龄的增长而减慢,”桑塔格说。“因此,随着时间的推移,衰老的细胞无法快速或有效地清除所有垃圾,错误折叠的蛋白质在细胞内积累得越来越多。
“我们发现核和细胞质质量控制途径通过核包膜进行交流,核包膜是一种因衰老和神经退行性疾病而受损的结构,”Frydman说。“许多导致过早衰老的早衰突变体会扭曲核包膜。这项工作确实改变了游戏规则,最终带来了一种新的方法来理解并治愈影响日益老龄化人口的各种可怕疾病。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【禁不住念什么】在日常生活中,我们常常会遇到一些词语让人“禁不住”去读、去想,甚至去写。其中,“禁不住...浏览全文>>
-
【禁闭岛结局】《禁闭岛》(英文名:Shutter Island)是一部由马丁·斯科塞斯执导,莱昂纳多·迪卡普里奥主演...浏览全文>>
-
【禁闭岛的结局真相】《禁闭岛》(英文名:Shutter Island)是一部由马丁·斯科塞斯执导,莱昂纳多·迪卡普里...浏览全文>>
-
【靳字怎么读】在日常生活中,我们经常会遇到一些不常见的汉字,这些字不仅发音复杂,含义也常常让人感到困惑...浏览全文>>
-
【靳这个字怎么念】“靳”是一个较为少见的汉字,常用于人名或姓氏中。对于不熟悉该字的人来说,可能会不知道...浏览全文>>
-
【靳怎么读音】“靳”是一个较为少见的汉字,常出现在人名或地名中。对于不熟悉这个字的人来说,可能会对其读...浏览全文>>
-
【靳东个人资料】靳东是中国内地著名的男演员,因在多部影视作品中表现出色而广受观众喜爱。他以沉稳的气质、...浏览全文>>
-
【靳东的妹妹为什么叫高露】很多人对“靳东的妹妹为什么叫高露”这一问题感到疑惑,因为从名字上看,似乎“高...浏览全文>>
-
【金枝玉叶剧情简介】《金枝玉叶》是一部以民国时期为背景的都市情感剧,讲述了出身名门的女主角在家族、爱情...浏览全文>>
-
【金枝玉叶花语是什么】“金枝玉叶”是一种常见的观赏植物,因其叶片厚实、色泽翠绿、形态美观而广受喜爱。在...浏览全文>>
